《2022年高中化學(xué) 2.1《元素與物質(zhì)的分類(3)》教案 魯科版必修1》由會員分享�,可在線閱讀,更多相關(guān)《2022年高中化學(xué) 2.1《元素與物質(zhì)的分類(3)》教案 魯科版必修1(4頁珍藏版)》請在裝配圖網(wǎng)上搜索���。
1�、2022年高中化學(xué) 2.1《元素與物質(zhì)的分類(3)》教案 魯科版必修1
一.教材分析
(一)知識脈絡(luò)
學(xué)生在初中化學(xué)中已經(jīng)認(rèn)識了幾種具體物質(zhì)的性質(zhì)和單質(zhì)�����、酸�、堿、鹽�、氧化物的一般性質(zhì),但他們只是從單個物質(zhì)的角度認(rèn)識物質(zhì)的性質(zhì)���,尚未從一類物質(zhì)的角度認(rèn)識物質(zhì)的性質(zhì)�,更未建立起元素與物質(zhì)的關(guān)系�����。因此�,通過元素與物質(zhì)的關(guān)系的研究,引導(dǎo)學(xué)生以元素的觀點認(rèn)識物質(zhì)�����;通過研究用不同的標(biāo)準(zhǔn)對物質(zhì)進行分類�,使學(xué)生建立分類的觀點。在分類的基礎(chǔ)上�����,研究純凈物——單質(zhì)���、氧化物���、酸、堿�、鹽之間的相互關(guān)系;在學(xué)生原有的認(rèn)知結(jié)構(gòu)中已存在溶液�����、濁液等混合物的觀點�,進而引進一種新的混合物——膠體,建立分散系的概念�����,豐富學(xué)生
2、對混合物的認(rèn)識���,并使學(xué)生了解膠體的一般性質(zhì)��,學(xué)會從粒度大小的角度對混合物進行分類��。
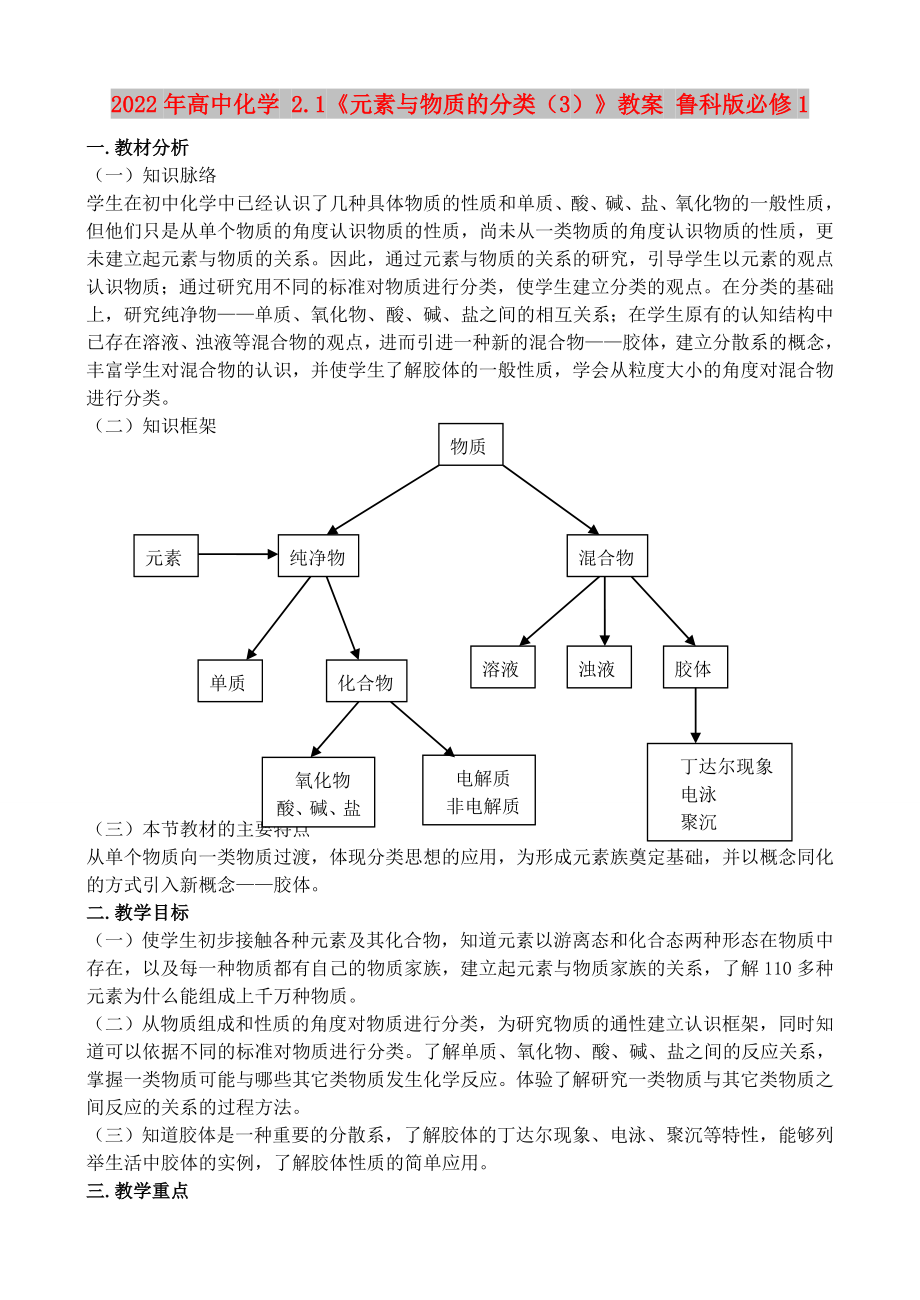
物質(zhì)
元素
純凈物
混合物
單質(zhì)
化合物
溶液
濁液
膠體
氧化物
酸����、堿�����、鹽
電解質(zhì)
非電解質(zhì)
丁達(dá)爾現(xiàn)象
電泳
聚沉
(二)知識框架
(三)本節(jié)教材的主要特點
從單個物質(zhì)向一類物質(zhì)過渡�����,體現(xiàn)分類思想的應(yīng)用�,為形成元素族奠定基礎(chǔ),并以概念同化的方式引入新概念——膠體���。
二.教學(xué)目標(biāo)
(一)使學(xué)生初步接觸各種元素及其化合物��,知道元素以游離態(tài)和化合態(tài)兩種形態(tài)在物質(zhì)中存在�,以及每一種物質(zhì)都有自己的物質(zhì)家族���,建立起元素與物質(zhì)家族的關(guān)系���,了解
3、110多種元素為什么能組成上千萬種物質(zhì)����。
(二)從物質(zhì)組成和性質(zhì)的角度對物質(zhì)進行分類,為研究物質(zhì)的通性建立認(rèn)識框架���,同時知道可以依據(jù)不同的標(biāo)準(zhǔn)對物質(zhì)進行分類���。了解單質(zhì)、氧化物���、酸����、堿、鹽之間的反應(yīng)關(guān)系����,掌握一類物質(zhì)可能與哪些其它類物質(zhì)發(fā)生化學(xué)反應(yīng)。體驗了解研究一類物質(zhì)與其它類物質(zhì)之間反應(yīng)的關(guān)系的過程方法��。
(三)知道膠體是一種重要的分散系�����,了解膠體的丁達(dá)爾現(xiàn)象����、電泳、聚沉等特性���,能夠列舉生活中膠體的實例�,了解膠體性質(zhì)的簡單應(yīng)用�����。
三.教學(xué)重點
(一)知識與技能:元素與物質(zhì)的關(guān)系���;膠體的性質(zhì)�����。
(二)過程與方法:探討各類物質(zhì)的通性及其相互反應(yīng)關(guān)系����,學(xué)會如何以元素為核心認(rèn)識物質(zhì),從多角度
4��、依據(jù)不同標(biāo)準(zhǔn)對物質(zhì)進行分類并體驗分類的重要意義����。
(三)情感態(tài)度與價值觀:體會分類的重要意義��,依據(jù)不同的標(biāo)準(zhǔn)對物質(zhì)進行分類��;讓學(xué)生樹立運用化學(xué)知識���,使自己生活得更健康���。
四.教學(xué)準(zhǔn)備
(一)學(xué)生準(zhǔn)備
要求學(xué)生復(fù)習(xí)初中化學(xué)中單質(zhì)、氧化物�����、酸、堿���、鹽之間的關(guān)系���,復(fù)習(xí)第一章第二節(jié)研究物質(zhì)性質(zhì)的方法和程序,為學(xué)習(xí)本節(jié)教材做準(zhǔn)備�����。
(二)教師準(zhǔn)備
教學(xué)媒體及課件��;概念圖�����;實驗探究的藥品及儀器�。
五.教學(xué)方法與學(xué)習(xí)方法:教學(xué)方法——引導(dǎo)探究法;學(xué)習(xí)方法——合作學(xué)習(xí)法���。
六.課時計劃:3課時
七.教學(xué)過程
【板書】 第一節(jié) 元素與物質(zhì)的分類
5���、第3課時
引入新課——
聯(lián)想·質(zhì)疑(提出問題)
在天氣晴朗的情況下,當(dāng)你漫步在茂密的樹林里�����,會看到縷縷霞光穿過林木枝葉鋪灑在地面上,你知道這是為什么嗎��?
在晚上����,當(dāng)你打開手電筒時,會看到一道“光柱”射向天空或射向遠(yuǎn)方��,你知道這是為什么嗎����?
這些現(xiàn)象與一種特殊的混合物有關(guān)��。
1.分散質(zhì):被分散成微粒的物質(zhì)叫分散質(zhì)����。如食鹽溶液中的食鹽。
2.分散劑:分散質(zhì)分散到另一種物質(zhì)中��,這種物質(zhì)(另一種物質(zhì))叫分散劑���。如食鹽溶液中的水�����。
3.分散系:由分散質(zhì)和分散劑構(gòu)成的混合物統(tǒng)稱為分散系���。如食鹽溶液就是一種分散系����。
教師要求學(xué)生列舉幾種分散系����,并指出分散質(zhì)和分散劑。
4.幾種常見的分散系
6�、(根據(jù)分散系中分散質(zhì)粒度大小進行分類)
(1)溶液:分散質(zhì)是分子或離子,分散質(zhì)的粒度<1nm(10-9m)���,具有透明���、均勻、穩(wěn)定的宏觀特征��。
(2)濁液:分散質(zhì)是分子的集合體或離子的集合體�,分散質(zhì)的粒度>100nm(10—7m),具有渾濁�����、不穩(wěn)定等宏觀特征。
(3)膠體:分散質(zhì)的粒度介于1~100nm之間的分散系叫膠體(也稱為溶膠)����。
濁液
100nm
膠體
1nm
溶液
【點評】數(shù)軸是初一數(shù)學(xué)中的一個重要內(nèi)容。在化學(xué)教學(xué)中應(yīng)用數(shù)軸將同一類型的不同對象按數(shù)量的大小在數(shù)軸上進行有序排列���,可以使學(xué)生建立有序思維�����。如物質(zhì)的溶解性(難溶�����、微溶、易溶)���、同種元素的變價化合物均可
7����、用數(shù)軸進行排列����。
5.膠體的性質(zhì)
(1)丁達(dá)爾現(xiàn)象:當(dāng)可見光束通過膠體時���,在入射光側(cè)面可觀察到明亮的光區(qū),這種現(xiàn)象叫做丁達(dá)爾現(xiàn)象或丁達(dá)爾效應(yīng)��。
丁達(dá)爾現(xiàn)象產(chǎn)生的原因:膠體中分散質(zhì)微粒對可見光(波長為400~700nm)散射而形成的��。
丁達(dá)爾現(xiàn)象的應(yīng)用:區(qū)別溶液和膠體���。
實驗:先取一個具有雙通性質(zhì)的紙筒(事先在紙筒的下端鉆一個小孔�,以讓光線通過)��,將紙筒套在盛在氫氧化鐵膠體的燒杯上��,再取一只40W的電燈泡�����,通電后放在紙筒的小孔處���,人從紙筒的上端從上往下觀察�,即可觀察到有一條“光亮的通路”的現(xiàn)象。
能同樣的辦法觀察食鹽溶液的現(xiàn)象�����。
(2)電泳:膠體中的分散質(zhì)微粒在直流電的作用下產(chǎn)生定
8��、向移動的現(xiàn)象叫電泳��。
電泳現(xiàn)象說明膠體中的分散質(zhì)微粒帶有電荷����。
膠體粒子帶電的經(jīng)驗規(guī)律——
帶正電荷的膠體粒子:金屬氫氧化物(如氫氧化鋁、氫氧化鐵膠體)���;金屬氧化物膠體���。
帶負(fù)電荷的膠體粒子:非金屬氧化物膠體;金屬硫化物膠體���;硅酸膠體�;土壤膠體��。
特殊膠體:AgI膠體粒子隨AgNO3和KI 的相對量不同可帶正電或負(fù)電�。若KI過量����,則AgI膠體粒子吸附I—而帶負(fù)電荷���;若AgNO3過量,則AgI膠體粒子吸附Ag+而帶正電荷�����。
(3)聚沉:向膠體中加入鹽時�����,其中的陽離子或陰離子能中和分散質(zhì)微粒所帶的電荷���,從而使分散質(zhì)聚集成較大的微粒���,在重力作用下形成沉淀析出。這種膠體形成沉淀析出的現(xiàn)象稱
9�、為膠體的聚沉(適用于液溶膠)。
實驗:向氫氧化鐵膠體中加入適量的硫酸鈉�����,可觀察到氫氧化鐵沉淀析出。
6.膠體的制備
凝聚法:
(1)向沸水中滴加幾滴飽和的氯化鐵溶液��,適當(dāng)加熱即可形成氫氧化鐵膠體(注意加熱時間不宜過長���,否則會形成氫氧化鐵沉淀)�。
FeCl3 +3H2O ====Fe(OH)3(膠體) +3HCl
(2)在不斷振蕩的情況下����,向稀KI溶液中加入稀AgNO3溶液,可制得淺黃色的確良AgI膠體��。
7.膠體的用途:
(1)鹽鹵點豆腐���;
(2)肥皂的制取和分離���;
(3)明礬凈水;
(4)FeCl3溶液用于傷口止血��。
(5)水泥硬化�����;
(6)冶金廠大量煙塵用高壓電除
10�、去�。
(7)土壤膠體中離子的吸附和交換過程��,保肥作用�����。
知識點擊:供學(xué)生閱讀�,并可讓學(xué)生進行家庭小實驗��,研究膠體提純的方法——滲析���。
家庭小實驗——用一個豬膀胱盛食鹽溶液和淀粉溶膠��,然后將豬膀胱浸泡在蒸餾水中�,過一段時間后���,用兩個試管分別取燒杯中的蒸餾水少許���,分別滴加硝酸酸化的AgNO3溶液碘水溶液,分別觀察產(chǎn)生的現(xiàn)象�����,并思考產(chǎn)生這兩種現(xiàn)象的原因。
8.三種分散系的比較
分散系
溶液
膠體
濁液
分散質(zhì)粒子的直徑
<1nm
1nm100nm
>100nm
外觀
均一����、透明
較均一、透明
不均一�����、不透明
分散質(zhì)微粒
分子����、離子
分子集合體、高分子
大量的分
11�����、子集合體
能否透過濾紙
能
能
不能
能否透過半透膜
能
不能
不能
穩(wěn)定性
穩(wěn)定
較穩(wěn)定
不穩(wěn)定
【點評】比較法是進行歸納總結(jié)的一種重要方法��。它能幫助學(xué)生找出不同對象的相同點和不同點��,抽象出不同事物的本質(zhì)特征���。學(xué)生自己建立表格進行比較則效果更好��。
課外作業(yè):
1.完成P36的知識結(jié)構(gòu)示意圖���。
2.P37第2題���。
【點評】教師利用本節(jié)教材引導(dǎo)學(xué)生研究元素與物質(zhì)的關(guān)系,探討物質(zhì)分類的方法��,并以常見的單質(zhì)�、氧化物���、酸����、堿����、鹽的代表物,著重探究它們之間的關(guān)系�����,能夠體現(xiàn)科學(xué)探究的一般過程�����。在研究純凈物之間的關(guān)系的基礎(chǔ)上,又從粒度大小的角度對混合物進行分類�,并以概念同化的方式引入“膠體”和分散系等概念,使學(xué)生明確分散系是上位概念�����,溶液��、膠體����、濁液是下位概念,它們之間存在大概念和小概念之間的包容關(guān)系�����。
 2022年高中化學(xué) 2.1《元素與物質(zhì)的分類(3)》教案 魯科版必修1
2022年高中化學(xué) 2.1《元素與物質(zhì)的分類(3)》教案 魯科版必修1