《中考化學(xué)專題復(fù)習(xí) 題型突破(二)曲線圖像題練習(xí) 新人教版》由會員分享,可在線閱讀���,更多相關(guān)《中考化學(xué)專題復(fù)習(xí) 題型突破(二)曲線圖像題練習(xí) 新人教版(7頁珍藏版)》請?jiān)谘b配圖網(wǎng)上搜索�����。
1、中考化學(xué)專題復(fù)習(xí) 題型突破(二)曲線圖像題練習(xí) 新人教版
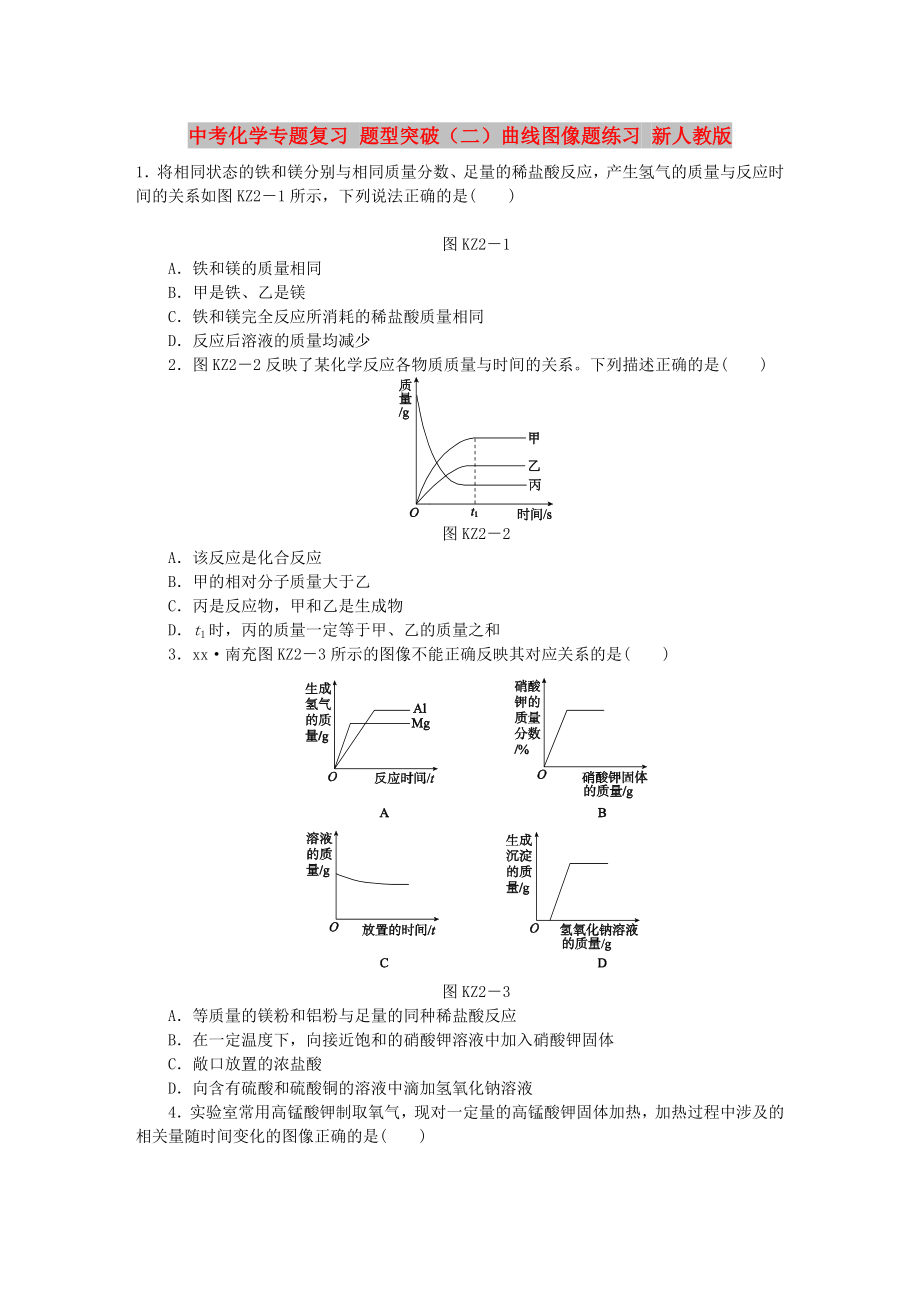
1.將相同狀態(tài)的鐵和鎂分別與相同質(zhì)量分?jǐn)?shù)��、足量的稀鹽酸反應(yīng)����,產(chǎn)生氫氣的質(zhì)量與反應(yīng)時(shí)間的關(guān)系如圖KZ2-1所示,下列說法正確的是( )
圖KZ2-1
A.鐵和鎂的質(zhì)量相同
B.甲是鐵�����、乙是鎂
C.鐵和鎂完全反應(yīng)所消耗的稀鹽酸質(zhì)量相同
D.反應(yīng)后溶液的質(zhì)量均減少
2.圖KZ2-2反映了某化學(xué)反應(yīng)各物質(zhì)質(zhì)量與時(shí)間的關(guān)系。下列描述正確的是( )
圖KZ2-2
A.該反應(yīng)是化合反應(yīng)
B.甲的相對分子質(zhì)量大于乙
C.丙是反應(yīng)物�,甲和乙是生成物
D.t1時(shí)���,丙的質(zhì)量一定等于甲�����、乙的質(zhì)量之和
3.xx·南充圖KZ2
2、-3所示的圖像不能正確反映其對應(yīng)關(guān)系的是( )
圖KZ2-3
A.等質(zhì)量的鎂粉和鋁粉與足量的同種稀鹽酸反應(yīng)
B.在一定溫度下����,向接近飽和的硝酸鉀溶液中加入硝酸鉀固體
C.敞口放置的濃鹽酸
D.向含有硫酸和硫酸銅的溶液中滴加氫氧化鈉溶液
4.實(shí)驗(yàn)室常用高錳酸鉀制取氧氣�����,現(xiàn)對一定量的高錳酸鉀固體加熱���,加熱過程中涉及的相關(guān)量隨時(shí)間變化的圖像正確的是( )
圖KZ2-4
5.圖KZ2-5所示的有關(guān)量的變化圖像與其對應(yīng)敘述相符的是( )
圖KZ2-5
6. KZ2-6所示圖像能正確反映其對應(yīng)關(guān)系的是( )
圖KZ2-6
A.①某溫度下�,向一定量的硝酸鉀
3�����、不飽和溶液中不斷加入硝酸鉀晶體
B.②在兩份等質(zhì)量、等溶質(zhì)質(zhì)量分?jǐn)?shù)的過氧化氫溶液中�,一份加催化劑,一份不加催化劑
C.③通電使水分解
D.④向盛有等質(zhì)量�����、等溶質(zhì)質(zhì)量分?jǐn)?shù)的過量稀硫酸的兩支試管中���,分別加入鎂和鋁
7.下列四個(gè)圖像中����,能正確反映變化關(guān)系的是( )
圖KZ2-7
8.下列圖像中�,能正確反映其對應(yīng)變化關(guān)系的是( )
圖KZ2-8
A.加熱等質(zhì)量的氯酸鉀制取氧氣
B.向一定質(zhì)量的燒堿溶液中加稀鹽酸
C.實(shí)驗(yàn)室高溫加熱一定質(zhì)量的石灰石
D.向一定質(zhì)量的硝酸銀溶液中加銅粉
9. KZ2-9所示的四個(gè)圖像�,能正確反映對應(yīng)變化關(guān)系的是( )
圖KZ
4、2-9
A.鎂在氧氣中燃燒
B.向二氧化錳中加入過氧化氫溶液
C.向一定質(zhì)量鐵粉和銅粉的混合物中加入硫酸銅溶液
D.等質(zhì)量的鎂����、鋁分別與質(zhì)量分?jǐn)?shù)相等且足量的稀硫酸反應(yīng)
10.化學(xué)概念間有包含���、并列����、交叉等不同關(guān)系�。下列選項(xiàng)符合如圖KZ2-10所示關(guān)系的是( )
圖KZ2-10
選項(xiàng)
A
B
C
D
X
化合反應(yīng)
純凈物
物理變化
化學(xué)反應(yīng)
Y
氧化反應(yīng)
混合物
化學(xué)變化
化合反應(yīng)
11.圖KZ2-11為某化學(xué)反應(yīng)的微觀示意圖�,其中相同的球代表同種原子。下列說法正確的是( )
圖KZ2-11
A.反應(yīng)前后原子種類改變
B.反應(yīng)前后
5����、分子個(gè)數(shù)不變
C.反應(yīng)前后元素種類不變
D.分子在化學(xué)變化中不可分
12.已知“”“”“”分別表示X�、Y��、Z三種不同的氣體分子�,在一定條件下的變化如圖KZ2-12所示��,由圖示得到的下列信息中錯(cuò)誤的是( )
圖KZ2-12
A.在化學(xué)變化中����,分子一定發(fā)生改變
B.分子之間有間隔
C.該反應(yīng)可表示為4X+Y===2Z
D.一個(gè)Z分子由4個(gè)原子構(gòu)成
13.在宏觀�����、微觀和符號之間建立聯(lián)系是化學(xué)學(xué)科的特點(diǎn)?��,F(xiàn)有A����、B����、C�、D四種物質(zhì),其微觀示意圖如圖KZ2-13所示��。
圖KZ2-13
(1)A物質(zhì)相對分子質(zhì)量為________��。
(2)上述物質(zhì)中屬于單質(zhì)的是_____(
6��、填序號),屬于有機(jī)物的是________(填化學(xué)式)�。
(3)C物質(zhì)的一個(gè)分子是由________________________構(gòu)成的。
(4)寫出反應(yīng)A+B→C+D的化學(xué)反應(yīng)方程式:
________________________________________________________________________�����。
14.工業(yè)上用甲和乙反應(yīng)制備丙和丁���,其反應(yīng)的微觀示意圖如圖KZ2-14所示:
圖KZ2-14
(1)該化學(xué)變化中沒有發(fā)生改變的粒子是________(填“分子”或“原子”)�。
(2)寫出該反應(yīng)的化學(xué)方程式:____________________
7��、__________。
(3)該反應(yīng)中含氫元素的化合物有________種�;反應(yīng)前后化合價(jià)發(fā)生變化的元素是________(填元素符號)����。
15.小明測得石灰石與一定量的稀鹽酸反應(yīng)后的溶液pH為2��,取適量該溶液向其中逐滴加入碳酸鈉溶液�,
圖KZ2-15
并測得溶液pH隨加入碳酸鈉溶液體積的變化曲線如圖KZ2-15所示����。請回答下列問題。
(1)A點(diǎn)處溶液中的兩種溶質(zhì)是__________________(寫化學(xué)式)���。
(2)AB段可觀察到的實(shí)驗(yàn)現(xiàn)象是____________。
(3)BC段發(fā)生反應(yīng)的化學(xué)方程式是________________________________
8�、______。
(4)CD段pH上升的原因是______________________________�。
16.xx·遵義請按要求完成下列金屬性質(zhì)的實(shí)驗(yàn)。
研究一:金屬與酸反應(yīng)過程中的能量變化�����。
(1)打磨后的鎂條與稀鹽酸反應(yīng)����,試管外壁發(fā)燙,說明該反應(yīng)________(填“放熱”或“吸熱”)�,反應(yīng)的化學(xué)方程式為______________________________�。
(2)實(shí)驗(yàn)測得反應(yīng)中產(chǎn)生氣體的速度(v)與時(shí)間(t)的關(guān)系如圖KZ2-16所示,請根據(jù)t1~t2時(shí)間段反應(yīng)速率變化,說明化學(xué)反應(yīng)速率受________等因素影響�����。
圖KZ2-16
研究二:金屬與鹽溶液反應(yīng)
9����、過程中的相關(guān)變化�。
(1)某同學(xué)用硫酸銅溶液把“鐵勺”變“銅勺”��,其反應(yīng)的化學(xué)方程式為________________________________________________________________________
______________________��。
(2)在一定量的AgNO3和Cu(NO3)2的混合溶液中加入鐵粉�����,充分反應(yīng)后,圖KZ2-17描述的相關(guān)變化曲線�,一定不正確的是________��。
圖KZ2-17
參考答案
1.C [解析] 根據(jù)試題提供的信息可知�����,生成的氫氣質(zhì)量相同,可以得到反應(yīng)的稀鹽酸的質(zhì)量是相同的��;消耗的金屬鎂的質(zhì)量小于金屬
10���、鐵的質(zhì)量����;根據(jù)圖像可知甲生成氫氣的速率快��,甲為較活潑金屬���,甲是鎂��,乙是鐵�。
2.C
3.B
4.D [解析] 加熱高錳酸鉀放出氧氣����,固體的質(zhì)量減少���,當(dāng)反應(yīng)完,固體質(zhì)量不再變化�;加熱高錳酸鉀��,剛開始沒有氧氣放出����,當(dāng)高錳酸鉀完全分解時(shí)不再生成氧氣���;加熱一定質(zhì)量的高錳酸鉀����,錳元素的質(zhì)量不變����,剛開始��,錳元素的質(zhì)量分?jǐn)?shù)不為0��。
5.D 6.A
7.A [解析] 向一定質(zhì)量的稀硫酸中加入鋅片����,鋅和硫酸反應(yīng),生成硫酸鋅和氫氣����,溶液質(zhì)量增加�����,完全反應(yīng)后,溶液的質(zhì)量不變��;加熱高錳酸鉀固體�����,會生成氧氣���,導(dǎo)致固體質(zhì)量減少���,而反應(yīng)前后錳元素的質(zhì)量不變��,故錳元素的質(zhì)量分?jǐn)?shù)會增大��;二氧化錳在過氧化氫分解的過程中
11��、作催化劑,其質(zhì)量在反應(yīng)前后不會改變�����。
8.C 9.B 10.A 11.C
12.C [解析] 根據(jù)參加反應(yīng)的分子數(shù)和生成的分子數(shù)可知��,該反應(yīng)的表達(dá)式應(yīng)該為3X+Y===2Z。
13.(1)16 (2)B CH4
(3)兩個(gè)氧原子和一個(gè)碳原子
(4)CH4+2O2CO2+2H2O
14.(1)原子 (2)CH4+H2OCO+3H2 (3)2 C�、H
15.(1)HCl和CaCl2
(2)產(chǎn)生氣泡
(3)Na2CO3+CaCl2===2NaCl+CaCO3↓
(4)Na2CO3溶液顯堿性(合理即可)
16.研究一:(1)放熱 Mg+2HCl===MgCl2+H2↑ (2)溫度
12�����、
研究二:(1)CuSO4+Fe===FeSO4+Cu (2)B
[解析] 研究一:(1)打磨后的鎂條與稀鹽酸反應(yīng)�,試管外壁發(fā)燙�����,說明該反應(yīng)放熱�����,鎂與鹽酸反應(yīng)的化學(xué)方程式為Mg+2HCl===MgCl2+H2↑。(2)通過圖中的反應(yīng)速率可以看出�,在t1~t2時(shí)間段反應(yīng)速率加快,所以化學(xué)反應(yīng)速率受溫度等因素影響�。研究二:(2)由金屬活動性順序可知,鐵會先與硝酸銀反應(yīng)生成硝酸亞鐵和銀�����,然后再與硝酸銅反應(yīng)生成硝酸亞鐵和銅���。剛開始銅的質(zhì)量為0����,置換完銀才會置換出銅���;硝酸銅的質(zhì)量分?jǐn)?shù)最后會減小到0����;鐵和硝酸銀反應(yīng)生成硝酸亞鐵和銀�,每56份質(zhì)量的鐵會置換出216份質(zhì)量的銀,溶液質(zhì)量減輕�,鐵和硝酸銅反應(yīng)生成硝酸亞鐵和銅����,每56份質(zhì)量的鐵會置換出64份質(zhì)量的銅�,溶液質(zhì)量也會減輕,但是沒有前面減小的幅度大�����;鐵剛開始與硝酸銀反應(yīng)生成硝酸亞鐵和銀����,溶液中會出現(xiàn)銀離子、亞鐵離子�����、銅離子三種離子����,然后會出現(xiàn)亞鐵離子和銅離子�����,最后只剩下亞鐵離子����。
 中考化學(xué)專題復(fù)習(xí) 題型突破(二)曲線圖像題練習(xí) 新人教版
中考化學(xué)專題復(fù)習(xí) 題型突破(二)曲線圖像題練習(xí) 新人教版