《山東省淄博市臨淄區(qū)皇城鎮(zhèn)第二中學(xué)九年級(jí)化學(xué) 生活中的酸和堿課件 人教新課標(biāo)版》由會(huì)員分享�,可在線閱讀,更多相關(guān)《山東省淄博市臨淄區(qū)皇城鎮(zhèn)第二中學(xué)九年級(jí)化學(xué) 生活中的酸和堿課件 人教新課標(biāo)版(15頁(yè)珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索����。
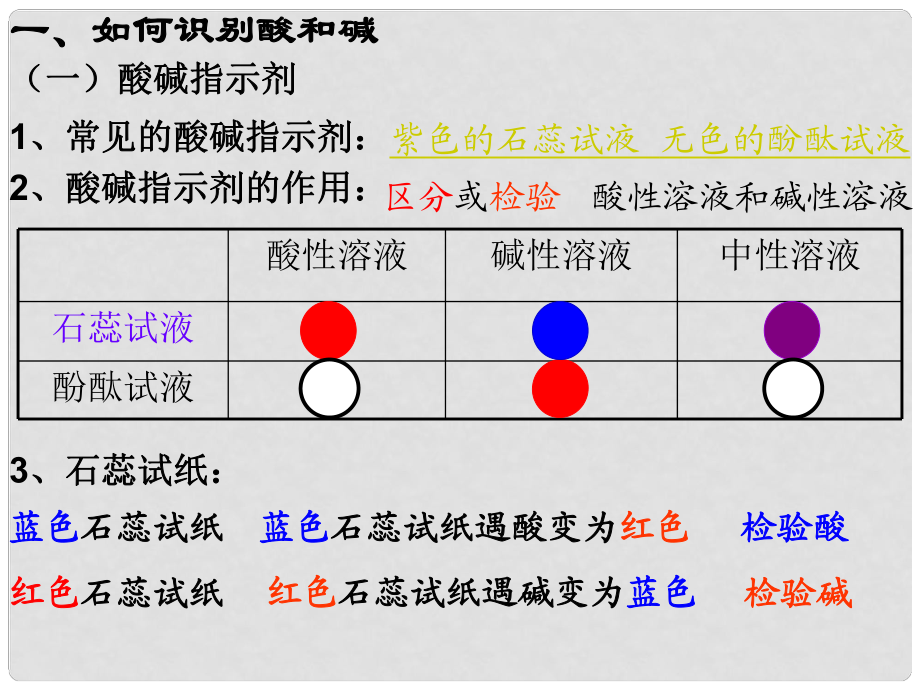
1、一、如何識(shí)別酸和堿一����、如何識(shí)別酸和堿(一)酸堿指示劑(一)酸堿指示劑1、常見的酸堿指示劑:�����、常見的酸堿指示劑:紫色的石蕊試液 無(wú)色的酚酞試液2�����、酸堿指示劑的作用:�、酸堿指示劑的作用:區(qū)分或檢驗(yàn) 酸性溶液和堿性溶液酸性溶液堿性溶液中性溶液石蕊試液酚酞試液3、石蕊試紙:���、石蕊試紙:藍(lán)色藍(lán)色石蕊試紙石蕊試紙紅色紅色石蕊試紙石蕊試紙檢驗(yàn)酸檢驗(yàn)酸檢驗(yàn)堿檢驗(yàn)堿藍(lán)色藍(lán)色石蕊試紙遇酸變?yōu)槭镌嚰堄鏊嶙優(yōu)榧t色紅色紅色紅色石蕊試紙遇堿變?yōu)槭镌嚰堄鰤A變?yōu)樗{(lán)色藍(lán)色為什么不同的酸的溶液都能使為什么不同的酸的溶液都能使石蕊試液石蕊試液變變紅紅��?不同的堿的溶液都能使不同的堿的溶液都能使石蕊試液石蕊試液變變藍(lán)藍(lán)�����?物質(zhì)的酸和
2�、堿的物質(zhì)的酸和堿的本質(zhì)區(qū)別本質(zhì)區(qū)別是什么��?是什么?交流共享交流共享硫酸硫酸H2SO4H+ �����、Cl- H+ ���、SO42-H+ H+ ��、SO42- 電離時(shí)生成的電離時(shí)生成的陽(yáng)陽(yáng)離子離子全部全部是氫離子是氫離子(H+)的化的化合物叫做酸�����。合物叫做酸����。 第一站:酸和堿第一站:酸和堿H+和和酸酸根根離離子子鹽酸鹽酸HCl 電離時(shí)生成的電離時(shí)生成的陰陰離子離子全部全部是氫氧根是氫氧根離子離子(OH-)的化合物叫做堿�����。的化合物叫做堿����。 第一站:識(shí)別酸和堿第一站:識(shí)別酸和堿氫氧化鉀氫氧化鉀KOH氫氧化鈉氫氧化鈉NaOHNa+ �����、OH- K+ 、OH- Na+ �、OH- K+ 、OH- 金金屬屬離離子子和和OH
3�、- 第一站:識(shí)別酸和堿第一站:識(shí)別酸和堿 選出所列選出所列物質(zhì)中的酸物質(zhì)中的酸和堿(填序和堿(填序號(hào))號(hào))酸:酸: 堿:堿:HNO3 NH4ClNa2SO4 H2CO3 Ca(OH)2 Ba(OH)2想一想:想一想:NaHSO4 屬于酸嗎?為什么����?屬于酸嗎?為什么�?原子團(tuán)原子團(tuán)氫氧根 OH硫酸根 SO4硝酸根 NO3碳酸根 CO3銨根 NH4常見原子團(tuán)的化合價(jià)常見原子團(tuán)的化合價(jià)負(fù)一硝酸氫氧根負(fù)一硝酸氫氧根 負(fù)二碳酸硫酸根負(fù)二碳酸硫酸根只有正一是銨根只有正一是銨根名稱名稱氫氧根氫氧根 硫酸根硫酸根 碳酸根碳酸根硝酸根硝酸根銨根銨根符號(hào)符號(hào)離子符離子符號(hào)號(hào)化合價(jià)化合價(jià)相應(yīng)的相應(yīng)的酸酸與與堿堿OHS
4、O4CO3NO3OH-SO42-H2SO4CO32-H2CO3NO3-HNO3NH4NH4+-1-2-2- 1+ 1NaOH分清常見化學(xué)用語(yǔ):分清常見化學(xué)用語(yǔ):NH3.H2OH+ OH-酸溶液酸溶液堿溶液堿溶液酸性酸性堿性堿性溶液酸堿性的強(qiáng)弱程度溶液酸堿性的強(qiáng)弱程度1. 1.溶液酸堿性強(qiáng)弱程度用溶液酸堿性強(qiáng)弱程度用表示表示溶液酸堿性的強(qiáng)弱程度跟什么有關(guān)���?溶液酸堿性的強(qiáng)弱程度跟什么有關(guān)���?pHpH的范圍如何規(guī)定?的范圍如何規(guī)定���?pHpH的大小與溶液酸堿性有什么關(guān)系�?的大小與溶液酸堿性有什么關(guān)系����?pHpH如何測(cè)定�?如何測(cè)定�����?閱讀提綱閱讀提綱一定量的水溶液中一定量的水溶液中H H+ +的數(shù)量越多����,酸性
5、越強(qiáng)�。的數(shù)量越多,酸性越強(qiáng)�����。一定量的水溶液中一定量的水溶液中OHOH- -的數(shù)量越多����,堿性越強(qiáng)����。的數(shù)量越多,堿性越強(qiáng)����。pHpH的范圍通常在的范圍通常在0 01414之間之間中性酸性逐漸增強(qiáng)酸性逐漸增強(qiáng)堿性逐漸增強(qiáng)堿性逐漸增強(qiáng)0 1 2 3 4 5 6 7 8 9 10 11 12 13 14pHpH7 溶液顯堿性溶液顯堿性溶液酸堿性的強(qiáng)弱程度溶液酸堿性的強(qiáng)弱程度1. 1.溶液酸堿性強(qiáng)弱程度用溶液酸堿性強(qiáng)弱程度用表示表示(pHpH的范圍通常在的范圍通常在0 01414之間)之間)中性酸性逐漸增強(qiáng)酸性逐漸增強(qiáng)堿性逐漸增強(qiáng)堿性逐漸增強(qiáng)2.pH2.pH的測(cè)定的測(cè)定 pHpH試紙?jiān)嚰?在玻璃片或白瓷板上
6��、放一片在玻璃片或白瓷板上放一片pH 試紙���,用玻璃棒蘸取被測(cè)試紙,用玻璃棒蘸取被測(cè)液滴到試紙上����,把試紙顯示的液滴到試紙上,把試紙顯示的顏色與標(biāo)準(zhǔn)比色卡比較���,即可顏色與標(biāo)準(zhǔn)比色卡比較�,即可得出被測(cè)液的得出被測(cè)液的pH ����。0 1 2 3 4 5 6 7 8 9 10 11 12 13 14pH2、溶液酸堿性的強(qiáng)弱�、溶液酸堿性的強(qiáng)弱(1)酸堿性的強(qiáng)弱)酸堿性的強(qiáng)弱(2)酸堿性強(qiáng)弱的表示:)酸堿性強(qiáng)弱的表示:pH(3)酸堿性強(qiáng)弱與)酸堿性強(qiáng)弱與pH的關(guān)系:的關(guān)系:一定量溶液一定量溶液 H+ 數(shù)量數(shù)量越多酸性越強(qiáng);越多酸性越強(qiáng)���; OH- 數(shù)量數(shù)量越多堿性越強(qiáng)越多堿性越強(qiáng)pHpH的范圍:的范圍:0 0141
7�����、4之間之間(1)pH=7 溶液顯中性溶液顯中性(2)pH7 溶液顯堿性溶液顯堿性pH越小�����,酸性越強(qiáng)越小����,酸性越強(qiáng)pH越大,堿性越強(qiáng)越大�,堿性越強(qiáng)酸性逐漸增強(qiáng)酸性逐漸增強(qiáng)0 1 2 3 4 5 6 7 8 9 10 11 12 13 14pH中性堿性逐漸增強(qiáng)堿性逐漸增強(qiáng)(4)pH的測(cè)定:的測(cè)定:pH試紙?jiān)嚰?在玻璃片或白瓷板上放一片在玻璃片或白瓷板上放一片pH pH 試紙,用試紙�,用玻璃玻璃棒蘸取棒蘸取被測(cè)液滴到試紙上,把試紙顯示的顏被測(cè)液滴到試紙上����,把試紙顯示的顏色與色與標(biāo)準(zhǔn)比色卡標(biāo)準(zhǔn)比色卡比較,得出被測(cè)液的比較�����,得出被測(cè)液的pH pH �����。三���、酸和堿對(duì)生命活動(dòng)的意義三���、酸和堿對(duì)生命活動(dòng)的意義1
8、 1�����、酸和堿與人的生理活動(dòng)密切相關(guān)����、酸和堿與人的生理活動(dòng)密切相關(guān)2 2����、土壤的酸堿性對(duì)植物的生長(zhǎng)非常重要����、土壤的酸堿性對(duì)植物的生長(zhǎng)非常重要人體某些體液的正常pH范圍血液唾液胃液乳汁尿液pH7.357.357.457.456.66.67.17.10.80.81.51.56.46.46.76.75.05.07.07.0大多數(shù)植物適宜在接近中性的土壤生長(zhǎng)西瓜西瓜6.06.07.07.0蘋果樹蘋果樹6.06.08.08.0小麥小麥6.06.07.07.0紫色石蕊紫色石蕊試液在不同溶液中的顏色變化試液在不同溶液中的顏色變化白醋白醋檸檬汁檸檬汁 石灰水石灰水 肥皂水肥皂水 食鹽水食鹽水 蔗糖水蔗糖水加入加
9、入紫色石蕊紫色石蕊試液后的顏色試液后的顏色酸性溶液酸性溶液中性溶液中性溶液堿性溶液堿性溶液紫色石蕊試液遇紫色石蕊試液遇酸酸變成變成紅色紅色紫色石蕊試液遇紫色石蕊試液遇堿堿變成變成藍(lán)色藍(lán)色紫色石蕊試液在紫色石蕊試液在中性中性溶液中仍為溶液中仍為紫色紫色無(wú)色酚酞試液在不同溶液中顏色變化無(wú)色酚酞試液在不同溶液中顏色變化白醋白醋檸檬汁檸檬汁 石灰水石灰水 肥皂水肥皂水 食鹽水食鹽水 蔗糖水蔗糖水加入無(wú)色酚酞加入無(wú)色酚酞試液后的顏色試液后的顏色酸性溶液酸性溶液中性溶液中性溶液堿性溶液堿性溶液無(wú)色酚酞試液遇酸不變色無(wú)色酚酞試液遇酸不變色無(wú)色酚酞試液遇無(wú)色酚酞試液遇堿堿變成變成紅色紅色無(wú)色酚酞試液在無(wú)色酚酞
10、試液在中性中性溶液中仍為溶液中仍為無(wú)色無(wú)色返回返回2����、溶液酸堿性的強(qiáng)弱、溶液酸堿性的強(qiáng)弱(1)酸堿性的強(qiáng)弱)酸堿性的強(qiáng)弱(2)酸堿性強(qiáng)弱的表示:)酸堿性強(qiáng)弱的表示:pH(3)酸堿性強(qiáng)弱與)酸堿性強(qiáng)弱與pH的關(guān)系:的關(guān)系:一定量溶液一定量溶液 H+ 數(shù)量數(shù)量越多酸性越強(qiáng)����;越多酸性越強(qiáng)�; OH- 數(shù)量數(shù)量越多堿性越強(qiáng)越多堿性越強(qiáng)pHpH的范圍:的范圍:0 01414之間之間(1)pH=7 溶液顯中性溶液顯中性(2)pH7 溶液顯堿性溶液顯堿性pH越小�����,酸性越強(qiáng)越小,酸性越強(qiáng)pH越大����,堿性越強(qiáng)越大,堿性越強(qiáng)酸性逐漸增強(qiáng)酸性逐漸增強(qiáng)0 1 2 3 4 5 6 7 8 9 10 11 12 13 14pH中性堿性逐漸增強(qiáng)堿性逐漸增強(qiáng)(4)pH的測(cè)定:的測(cè)定:pH試紙?jiān)嚰?在玻璃片或白瓷板上放一片在玻璃片或白瓷板上放一片pH pH 試紙,用試紙�����,用玻玻璃棒蘸取璃棒蘸取被測(cè)液滴到試紙上����,把試紙顯示的被測(cè)液滴到試紙上���,把試紙顯示的顏色與顏色與標(biāo)準(zhǔn)比色卡標(biāo)準(zhǔn)比色卡比較���,得出被測(cè)液的比較,得出被測(cè)液的pH pH 。
 山東省淄博市臨淄區(qū)皇城鎮(zhèn)第二中學(xué)九年級(jí)化學(xué) 生活中的酸和堿課件 人教新課標(biāo)版
山東省淄博市臨淄區(qū)皇城鎮(zhèn)第二中學(xué)九年級(jí)化學(xué) 生活中的酸和堿課件 人教新課標(biāo)版